Жизнь на Земле за миллиарды лет четко подстроилась под 24-часовой период оборота нашей планеты вокруг своей оси. Многие процессы в организме (сон и бодрствование, обмен веществ, гормональный уровень, температура тела и т.д.) привязаны ко «внутренним часам» организма, которые в свою очередь "тикают" с циркадной ритмичностью (от лат. circa — «вокруг, примерно, около» и dies — «день»).
Собственно, сам этот факт установлен давно и широко известен. И значение этих «внутренних часов» намного шире общеизвестного деления людей на «жаворонков» и «сов», в зависимости от пика суточной активности. Установлено, что наши биологические часы влияют на способность вирусов к распространению, и, вероятно в силу этого, в разное время суток организм по-разному подвержен инфекциям. Другой эксперимент показал, что искусственное продление светового дня может вызывать ожирение, а по мнению некоторых ученых, даже повысить риск развития онкологии.
Но про то, как устроены и работают эти часы, наука до последних лет знала намного меньше. И Нобелевскую премию получили как раз исследователи, чья работа помогла продвинуться в данном направлении.
Впервые ген, влияющий на циркадный ритм, идентифицировали в 1970-е годы Сеймур Бензер и Рональд Конопка, а в 1984 году нынешние лауреаты премии Джеффри Холл и Майкл Росбаш сумели изолировать и секвенировать его. В дальнейшем они показали, что белок PER, который кодирует этот ген, накапливается ночью и разрушается днем.
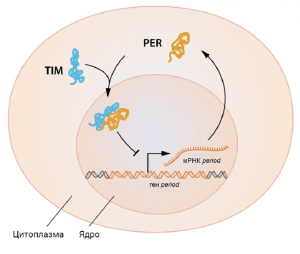 Причем, система «клеточных часов» регулирует сама себя: сначала белок PER накапливается в ядре и этим блокирует собственный синтез. Потом он начинает разрушаться, и процесс его синтеза запускается снова… А в 1994 году третий лауреат Майкл Янг открыл дополнительные гены и белки, которые обеспечивают бесперебойную работу этой системы. Как заявил главный редактор журнала Science Джереми Берг, «с помощью генетики и инструментов молекулярной биологии они нашли очень элегантный молекулярный механизм с петлей обратной связи, в которой белок контролирует собственную экспрессию».
Причем, система «клеточных часов» регулирует сама себя: сначала белок PER накапливается в ядре и этим блокирует собственный синтез. Потом он начинает разрушаться, и процесс его синтеза запускается снова… А в 1994 году третий лауреат Майкл Янг открыл дополнительные гены и белки, которые обеспечивают бесперебойную работу этой системы. Как заявил главный редактор журнала Science Джереми Берг, «с помощью генетики и инструментов молекулярной биологии они нашли очень элегантный молекулярный механизм с петлей обратной связи, в которой белок контролирует собственную экспрессию».
О том, какое значение эта работа имеет для дальнейшего развития науки и какие исследования в данном направлении проводят новосибирские ученые, мы попросили рассказать заместителя директора НИИ физиологии и фундаментальной медицины СО РАН по научной работе, д.м.н. Константина Даниленко.
– Если рассматривать хронобиологию, в которой и я работаю, то за последние десятилетия в ней было два серьёзных открытия, которые позволили ей перейти из разряда, так скажем, «несерьезных» в число всеми признанных научных направлений. И одно из них – это как раз эти внутриклеточные часы, которые регулируют многие жизненные процессы организма в соответствии с их циркадными ритмами. Как и то, что их работа основана не на каком-то отдельном гене, а на целой системе, ансамбле генов. Причем, этот часовой механизм присутствует не в каком-то одном органе, например, в головном мозге, он есть во всех клетках организма в целом.
– А каким было второе открытие?
 – Это открытие в сетчатке глаза фоторецепторов, отличных от палочек и колбочек. Оно тоже было сделано сравнительно недавно, в 2000 году. Эти рецепторы проводят в головной мозг информацию о смене дня и ночи неосознанно для человека. И, по сути, являются ключиком к системе этой циркадной регуляции работы организма. Может быть, со временем и это открытие будет удостоено Нобелевской премии, поскольку по своему значению оно вполне сопоставимо с первым.
– Это открытие в сетчатке глаза фоторецепторов, отличных от палочек и колбочек. Оно тоже было сделано сравнительно недавно, в 2000 году. Эти рецепторы проводят в головной мозг информацию о смене дня и ночи неосознанно для человека. И, по сути, являются ключиком к системе этой циркадной регуляции работы организма. Может быть, со временем и это открытие будет удостоено Нобелевской премии, поскольку по своему значению оно вполне сопоставимо с первым.
– После публикации новости о присуждении Нобелевской премии за открытие молекулярного механизма, регулирующего суточные ритмы организма, прозвучали прогнозы о том, что скоро наука научится управлять этими процессами. Насколько это осуществимо?
– Это задача для генной инженерии. И то, насколько мы в силах ее решить, будет определяться развитием этого направления в целом. Исследования ведутся на лабораторных животных, но пока об управлении биологическими часами на генном уровне говорить рано. У нас в НИИФФМ мы работаем несколько в ином направлении.
– И над какими задачами трудятся сегодня новосибирские хронобиологи?
– У нас есть ряд именно хронобиологических исследований, но они носят в большей степени прикладной характер. Допустим, какие разновидности «биологических часов» (с точки зрения генного полиморфизма) есть у разных людей, почему одни - «жаворонки», а другие - «совы», почему одни легче других адаптируются к смене часовых поясов и тому подобное. Одни исследования мы проводим самостоятельно, другие – совместно с коллегами из Москвы, Новосибирска, Сыктывкара, а также из других стран.
– А можете привести пример из числа последних результатов?
– Недавно мы (вместе с зарубежными коллегами) завершили большую исследовательскую работу по сопоставлению работы биологических часов на организменном уровне (или центральных биологических часов в гипоталамусе) и клетках кожи одного и того же человека. Для этого мы встраивали в один из генов в клетках кожи вирус, который продуцировал светящийся белок. И с его помощью фиксировали активность работы этого ансамбля генов «внутриклеточных часов». Исследования показали, что эти механизмы в клетках гипоталамуса и кожи работают синхронно. В результате, ранее, чтобы измерить «ход» биологических часов конкретного человека, его надо было помещать на несколько дней в условия низкого освещения. Теперь же нам, используя эту методику, достаточно взять у человека клетки кожи, поместить их в чашку Петри и провести там исследования, которые быстро и точно установят – «сова» он или «жаворонок» и ряд других важных параметров работы его биологических часов.
Наталья Тимакова
- Войдите или зарегистрируйтесь, чтобы отправлять комментарии

