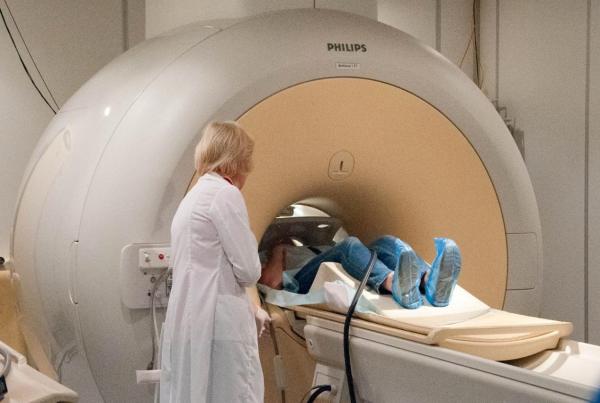
Коллаборация сибирских и монгольских исследователей во главе с Иркутским институтом химии им. А. Е. Фаворского СО РАН разрабатывает методы тераностики — одновременной терапии и диагностики — трудноизлечимых видов рака головного мозга (например, глиобластомы). В основе этих методов — полисахаридные нанобиокомпозиты, содержащие гадолиний и бор. Они способны накапливаться в опухоли и, как надеются ученые, позволят уничтожить ее с помощью светового инфракрасного воздействия, генератора нейтронов либо даже обычного МРТ-томографа.
«Проект, посвященный созданию магнитоуправляемых и люминесцентных средств для диагностики и лечения рака головного мозга, мы реализовываем в рамках комплексной программы СО РАН “Междисциплинарные интеграционные исследования на 2018—2020 годы”», — рассказывает координатор проекта заместитель директора по научной работе ИрИХ СО РАН кандидат химических наук Борис Геннадьевич Сухов.
Всё началось с того, что специалисты Восточно-Сибирского института медико-экологических исследований (Ангарск) совместно с учеными ИрИХ СО РАН обнаружили: некоторые природные макромолекулы полисахаридов, а именно — арабиногалактана, выделяемого из лиственницы сибирской, способны проникать через гематоэнцефалический барьер. Этот барьер между головным мозгом и кровеносной системой представляет собой совершенную защиту нашего «бортового компьютера» от всевозможных повреждений химическими токсигенами, вирусами и другими факторами. Однако именно из-за него большинство диагностических и лекарственных агентов не попадают в мозг, и о наличии, например, глиобластомы люди узнают уже на последних стадиях заболевания.
Ученым пришла идея внедрять в макромолекулы арабиногалактана специальные наночастицы, которые, во-первых, обладали бы магнитным или инфракрасным люминесцентным (в области прозрачности биотканей) сигналом и таким образом позволили бы осуществлять диагностику опухоли головного мозга. А во-вторых — были способны уже по другому лучевому сигналу уничтожать эту опухоль, нагревая ее до критических состояний и вызывая естественный апоптоз (самоубийство) онкоклеток либо провоцируя в ней под действием потока нейтронов ядерный нановзрыв. Кроме того, при влиянии на нанобиокомпозиты инфракрасного светового сигнала в области прозрачности биологических тканей могут генерироваться свободные радикалы — активные формы кислорода и азота, поражающие патогенные клетки уже по химическим каналам. Наиболее эффективно они уничтожают опухоли на ранних стадиях заболевания.
«Для проведения диагностики можно просто вводить нанобиокомпозиты в организм, где они распределяются и попадают в том числе в головной мозг, — зачастую этого уже достаточно, чтобы детализированно увидеть опухоль на МРТ. Другой способ — создать для наночастиц такую оболочку (например, полимерный сахар арабиногалактан), которую будут эффективно поглощать из кровотока именно онкоклетки. Тогда тераностический агент станет накапливаться в опухоли для последующего проведения терапии. Если препарат будет целенаправленно захвачен онкоклетками, то удару подвергнутся прежде всего они. Видя с помощью МРТ или люминесценции, где локализовано заболевание, мы можем селективно направлять магнитный, световой или нейтронный луч только туда и не воздействовать на здоровые клетки, в которых скоплено некоторое количество тераностического агента. Кроме того, за счет придания нанокомпозитным частицам магнитных свойств появляется возможность их перемещать, направлять, концентрировать и удерживать в опухоли под действием магнитного поля», — говорит Борис Сухов.
Помимо Иркутского института химии им. А. Е. Фаворского СО РАН в проекте участвуют еще четыре организации. Институт химии и химической технологии Монгольской академии наук ответственен за извлечение из возобновляемого сырья Монголии новых потенциальных макромолекул, способных преодолевать гематоэнцефалический барьер. Выделенные группы молекул передаются в ИрИХ СО РАН, и уже здесь в них генерируют наночастицы, способные давать диагностический сигнал и совершать терапевтическую работу.
В Восточно-Сибирском институте медико-экологических исследований работают специалисты в области токсикологии, фармакодинамики и фармакокинетики, которые изучают, как создаваемые тераностические наночастицы накапливаются, перераспределяются в организме, особенно в головном мозге, каким образом и с какой скоростью выводятся из него. «Общее представление у нас есть. Уже показано, что все созданные нами тераностические наноматериалы выводятся обычными путями соответствующими системами организма, и фатальных последствий не вызывают. Однако для каждого нового наноструктурированного соединения необходимы детальные исследования токсичности и безопасности», — комментирует Борис Сухов.
Сотрудники Института ядерной физики им. Г. И. Будкера СО РАН (Новосибирск) детализируют нейтронозахватные свойства нанобиокомпозитов, необходимые для терапии опухоли. «Мы делаем наночастицы, содержащие гадолиний и бор. Эти элементы, особенно их изотопы: бор-10 и гадолиний-157, обладают очень высокой вероятностью захвата нейтронов, она на 4—7 порядков больше, чем у всех других химических элементов живой ткани (что означает: нейтроны практически не будут повреждать здоровые клетки), — рассказывает исследователь. — При захвате нейтронов ядрами атомов бора и гадолиния получаются крайне нестабильные ядра, называемые компаунд-ядрами. Они проживут очень недолго, и затем произойдет ядерный взрыв. Результативность такой терапии будет гораздо больше, чем моноканальной, — с применением только бора или только гадолиния, поскольку это разные ядерные взрывы и их терапевтические повреждающие факторы тоже разные. Современные онкологические исследования показывают, что опухолевую клетку, уже имеющую или быстро приобретающую устойчивость к разнообразным факторам, гораздо легче уничтожить, применяя сразу несколько различных каналов повреждения.
Дополнительным преимуществом наноструктурированных средств для тераностики опухолей является тот факт, что каждая наночастица препарата будет содержать сразу тысячи атомов бора и гадолиния (тогда как применяющийся сегодня в медицине препарат борфенилаланин — только один атом бора), что резко повысит эффективность нейтронного захвата».
Гадолиний используется в препарате еще и для того, чтобы у композитных наночастиц были магнитные свойства, необходимые для МРТ-диагностики, а также чтобы перемещать, направлять, концентрировать и удерживать в опухоли наночастицы градиентным магнитным полем. Кроме того, это позволило бы с помощью переменного магнитного поля обычного томографа нагревать частицы и уничтожать глиобластому, не прибегая к ядерному взрыву.
«Если удастся сделать нагреваемость комплекса контролируемой, на начальных стадиях рака получится полностью удалять опухоль без вреда для организма: при температуре 43—47 °C включается естественный физиологический механизм самоубийства клетки — апоптоз, при котором ничего в организме не страдает, не поражаются токсинами печень, почки и другие защитные и выделительные органы», — говорит Борис Сухов.
Преимущество этой технологии и в том, что для нее не нужны громоздкие и дорогостоящие генераторы нейтронов. Терапию глиобластомы и других опухолей мозга можно будет осуществлять на обычных МР-томографах, которые сегодня есть практически в каждой серьезной клинике. Таким образом, доступность методики одновременной диагностики и терапии для онкобольных резко возрастет.
Детальное изучение магнитных характеристик всех разрабатываемых в проекте наноматериалов — задача Международного томографического центра СО РАН (Новосибирск). Там из синтезированных нанобиокомпозитов отбираются и испытываются те, которые наиболее подходят для МРТ-диагностики. Также в МТЦ СО РАН разрабатываются способы направлять, концентрировать, удерживать на опухоли наночастицы под действием магнитного поля и магнитотермически влиять на опухоль.
Сейчас проект находится на стадии фундаментальных исследований и доклинических испытаний наиболее перспективных образцов, до внедрения многоканального метода тераностики в клиническую онкологию еще далеко. Однако, по словам ученых, получаемые результаты обнадеживают. «Мы боялись, что у содержащих гадолиний наноматериалов будет наследоваться высокая токсичность этого химического элемента, но она оказалась умеренной. Выяснилось: в составе наночастиц, объединенных с биополимерами, например арабиногалактаном, гадолиний резко снижает негативное воздействие на организм. Это говорит о том, что подобные нанобиокомпозиты имеют большие перспективы, — отмечает исследователь. — Главное, что они способны проходить через гематоэнцефалический барьер. Обычно через него не проникают даже маленькие молекулы, а здесь он пропускает очень большие, по сравнению с простыми молекулами, наноразмерные образования. Представьте парадокс: в форточку, затянутую противомоскитной сеткой, не может попасть даже мельчайшая мошка, но в то же время спокойно проходит самовар. Для объяснения этого неординарного явления у нас есть гипотеза. Здесь, скорее всего, срабатывает свойство “открывать” клеточный гематоэнцефалический барьер, воздействуя на него локальными условиями наноосмоса, постоянно формирующимися в водном растворе вблизи особенной макромолекулы полисахарида арабиногалактана».
Осмос — это односторонняя диффузия растворителя, такого как вода, через естественную или искусственную полупроницаемую мембрану (перегородка, пропускающая только определенные растворенные вещества) в более концентрированный раствор.
«Этот наноосмос при приближении частицы нанобиокомпозита к гематоэнцефалическому барьеру делает его на время проницаемым. То есть синтезированную лиственницей макромолекулу полисахарида арабиногалактана в водном растворе можно рассматривать как жестко сцепленную нанокапельку концентрированного раствора углевода, способную проникнуть из кровотока в головной мозг через гематоэнцефалический барьер и пронести с собой в мозг всё, что в нее поместишь. Это наша рабочая гипотеза, но она находит подтверждение в более ранних исследованиях, а также в наших новых экспериментах», — говорит Борис Сухов.
Диана Хомякова
- Войдите или зарегистрируйтесь, чтобы отправлять комментарии