Кровеносная система лежит в основе функционирования головного мозга, и в области её работы ещё много «белых» пятен. Сибирские учёные в сотрудничестве с медиками решили устранить некоторые из них. Исследование имеет и прикладной выход: уже создана уникальная система мониторинга нейрохирургических операций, метод повышения качества магнитно-резонансной томографии, а также инструментарий для персонализированного моделирования протекания некоторых болезней.
Гемодинамика — это гидродинамика потока крови в сложной сети разветвлённых сосудов с различными свойствами стенок.
Эта работа стартовала в рамках гранта РНФ «Мозг и нейронауки», в котором для изучения того, как происходит течение крови в мозге, объединились специалисты различного профиля. Участники проекта: Институт гидродинамики им. М.А. Лаврентьева СО РАН, Институт теоретической и прикладной механики им. С.А. Христиановича СО РАН, ФИЦ Институт цитологии и генетики СО РАН, Международный томографический центр СО РАН, Новосибирский государственный университет, Владимирский государственный университет, Новосибирский научно-исследовательский институт патологии кровообращения имени академика Е.Н. Мешалкина и НИИ нейрохирургии им. Н.Н. Бурденко.
«Гемодинамика головного мозга имеет определяющее значение для всего того, что мы делаем. В конечном счёте, любое наше действие — движение рукой или какое-то интеллектуальное напряжение — есть результат того, что соответствующая зона, которая отвечает за эти функции, начинает более интенсивно снабжаться кровью. В результате запускается каскад различных реакций — биохимических, молекулярных, физиологических», — рассказывает сотрудник Института гидродинамики им. М.А. Лаврентьева доктор физико-математических наук Александр Павлович Чупахин.
С точки зрения гидродинамики эта система невероятно сложна, поскольку сосуды имеют различные прочностные свойства. Артерии упругие, вены более податливые — они дуются, когда в них повышается давление, а синусы (своеобразные коллекторы, по которым оттекает кровь) вообще проходят в твёрдой мозговой оболочке. Через всех них идёт пульсирующий поток крови.
«Мозг — очень энергоёмкий орган. Он составляет всего около 1,5% массы тела, но потребляет порядка 15% объема крови и 20% кислорода и глюкозы. Причём делает это что называется «с колёс»: в нём нет никаких запасов, «верблюжьих горбов». Именно поэтому прекращение кровоснабжения мозга неминуемо влечёт за собой нарушения», — говорит исследователь. По его словам, современная нейрохирургия обладает гораздо бОльшими возможностями по излечению болезней, обусловленных аномалиями в сосудистой системе мозга, нежели 10-15 лет назад.
На сегодняшний день сотрудники ННИИПК им. ак. Е.Н. Мешалкина успешно оперируют патологии головного мозга двух типов: артериовенозную мальформацию, при которой отсутствует молекулярная прослойка между артериальным и венозным деревом, из-за чего нарушается гидродинамический баланс. И артериальную аневризму — локальное выпячивание стенки артерии, в результате чего также сбивается нормальный кровоток.
Для излечения первой аномалии используется метод эмболизации артерио-венозной мальформации — по подводящему каналу доставляется специальное клеящее вещество, которое нейтрализует соответствующий участок с дефектными сосудами. От аневризмы избавляются путём выключения её из потока с помощью специальных приспособлений. Эти операции являются стандартными, в ННИИПК им. ак. Е. Н. Мешалкина их делают едва ли не каждый день, и в то же время они — на переднем крае медицины.
Однако врачи беспокоятся, что последствия этих вмешательств не всегда возможно предугадать: в одних случаях всё проходит успешно и пациент выздоравливает, в других почему-то начинаются осложнения, вплоть до кровоизлияния. В чём измерять эффективность нейрохирургической операции? Что нужно контролировать: скорость, давление, другое? В поисках ответов на эти вопросы медики обратились к учёным, а те попытались решить проблему с помощью системы преоперационного матмоделирования.
«Целью нашего проекта является комплексное исследование гемодинамики головного мозга в норме и при наличии аномалий для обнаружения законов движения крови, разработки методов управления кровотоком и создания алгоритмов предоперационного моделирования. Для этого необходимо получение надежных измеряемых данных, которое осложняется тем, что мы имеем дело с живым организмом», — комментирует Александр Павлович.
Сегодня благодаря проекту «Мозг и нейронауки» уже осуществляется мониторинг нейрохирургических операций на основе уникального американского прибора, разработанного для измерения давления и скорости в коронарных сосудах.
Учёные несколько усовершенствовали его и впервые в мире применили для исследования этих параметров в сосудах головного мозга. Разработка уже доведена до рекомендательных протоколов для нейрохирургических операций.
Система позволяет уточнить величину удельной нагрузки, во многих случаях отвечающую за успех хирургического вмешательства. «Когда происходит эмболизация артерио-венозной мальформации, то есть идёт «заделка» дефективного клубка сосудов, решающей величиной является удельная нагрузка, которая меняется в процессе операции, — отмечает Александр Чупахин. — Если она оказывается больше установленного значения, то существенно повышается риск разрыва этого клубка. Следуя такой рекомендации, можно достичь кратного уменьшения числа постоперационных осложнений». Процедура мониторинга, разработанная сибирскими исследователями, не имеет аналогов ни в России, ни в мире.
«Следующий проект, по которому мы работаем с виварием ИЦиГ СО РАН, — изучение фенотипа, генотипа и гемодинамики головного мозга для различных линий лабораторных животных по данным высокопольного ЯМР-сканирования. Постановка задачи здесь также является новой, и мы располагаем большим лабораторным массивом для этих исследований», — говорит Александр Павлович.
Магнитно-резонансная томография – неразрушающий метод исследования внутренней структуры объектов. В основе лежит явление ядерного магнитного резонанса (ЯМР) и метод спектроскопии, позволяющий определять физические и химические свойства молекул.
Когда учёные занялись мышами и стали создавать для них сети сосудов головного мозга, обнаружилось, что стандартный подход к построению не даёт цельной 3D картинки, но приводит лишь к фрагментаризации. Проблема в том, что сканирующая плоскость часто проходит под большим углом к сосуду, из-за чего расход крови может показаться меньше, чем он есть на самом деле.
Исследователи предложили метод варьирования наклона сканирующей плоскости. Результаты экспериментов уже подтвердили его эффективность. «На различных линиях лабораторных животных мы строим модели сосудов головного мозга, на которых можно потом прокручивать гемодинамику и смотреть на исходную задачу о её связи с фенотипом и генотипом», — комментирует учёный.
Клинические данные, снимаемые во время нейрохирургических операций, имеют некое ограниченное поле применения, поскольку нельзя варьировать давление или скорость кровотока в сосудах головного мозга. Однако это можно делать в лабораторных исследованиях на экспериментальных установках, которые конструируются в Международном томографическом центре СО РАН. На основе полученных данных затем строятся математические модели.
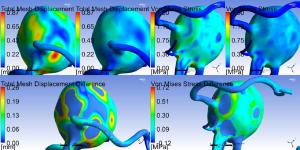 На сегодняшний день на приборном комплексе, состоящем из насоса и томографов, уже осуществлено экспериментальное исследование течения жидкости в силиконовой модели сонной артерии, и в дальнейшем метод может быть использован для получения достоверных данных при изучении кровотока.
На сегодняшний день на приборном комплексе, состоящем из насоса и томографов, уже осуществлено экспериментальное исследование течения жидкости в силиконовой модели сонной артерии, и в дальнейшем метод может быть использован для получения достоверных данных при изучении кровотока.
Также, основываясь на клинических данных ННИИПК им. ак. Е. Н. Мешалкина, учёные выяснили, что дифференциальное уравнение типа обобщенного осциллятора Ван дер Поля хорошо описывает связь между давлением и скоростью крови в сложной системе головного мозга, и создали на его основе метод медицинской диагностики. Модель позволяет прогнозировать поведение одной величины по поведению другой и демонстрирует различные нелинейные эффекты в окрестностях сосудистых патологий (оказалось, что здоровые сосуды относительно просты, а аномалия формирует некоторые особенности сложного поведения кровотока). Метод годится как для пациентов с артерио-венозной мальформацией, так и для людей с артериальной аневризмой.
Помимо вышеперечисленного сибирские учёные разрабатывают математический и компьютерный инструментарий для персонализированного моделирования гемодинамики церебральных аневризм. Его цель — определить особенности кровотока, оценить риск разрыва аневризмы или послеоперационного осложнения и, таким образом, скорректировать тактику лечения.
«У сосудов могут быть жёсткие стенки, либо односторонняя гидроупругость, когда кровь начинает деформировать стенки сосудов, либо реальная гидроупругость, при которой эта деформация вызывает изменение потока. Мы проводим моделирование по всем этим трём случаям. Расчёты проводятся на базе информационно-вычислительного центра НГУ, — говорит Александр Чупахин. — Ставился вопрос: как определить риск разрыва аневризмы, какая величина его характеризует? К экспериментальным данным мы применили алгоритмы численного моделирования, и было обнаружено, что здесь главную роль играют не локальные параметры, а энергетические. Нужно считать среднюю энергию на единицу объёма. Эта величина оказалась минимальной как раз для тех аневризм, где произошёл разрыв».
«Надёжные клинические и экспериментальные данные являются основой для математического моделирования, они потом возвращаются в биологию, медицину в виде каких-то рекомендаций и выводов. Потенциал не исчерпан. Исследование гемодинамики можно применять и для решения более сложных физиологических и когнитивных задач, потому что она лежит в основе распределения крови по сосудам, а значит — и в основе функционирования тех или иных зон головного мозга», — заключил учёный.
Диана Хомякова
Фото Юлии Поздняковой (1) и из презентации Александра Чупахина
- Войдите или зарегистрируйтесь, чтобы отправлять комментарии

